3月25日,欧盟发布了第18次NB调查结果,覆盖MDR/IVDR NB共计52家,数据截至2025年10月。方糖将着重讨论IVDR的非伴随诊断 (CDx) 部分。

丨申请量大涨,但质量堪忧
截至去年10月,共有19家机构获得IVDR NB资格。全部NB收到的IVDR总申请量已逾3634份,颁发的证书为2194张。表面上看,市场正在加速从旧指令向新法规过渡。然而,只有7家NB认为超半数的申请材料是完整的。 意即,大部分提交的文件都存在严重缺陷。
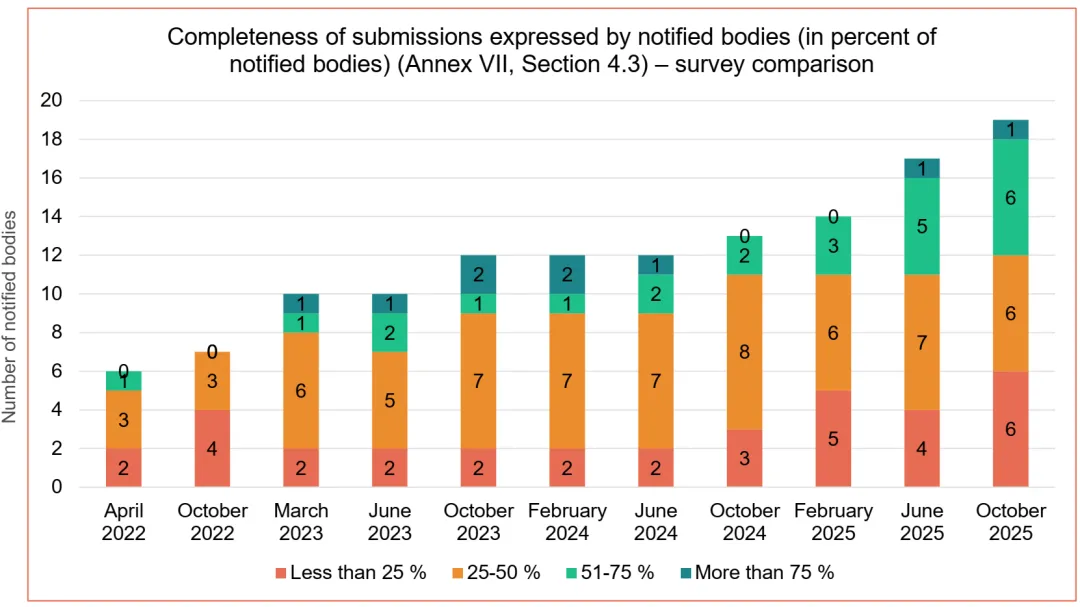
很多国内企业习惯了快速注册和模板化文档,但IVDR要求的是结合产品特征的全生命周期的技术文档:从设计开发到风险管理、从性能评估到上市后监督,每一部分都必须经得起推敲。
丨D类放量,EURL成了新瓶颈
在所有IVDR申请中,D类产品约占30%,申请量达到1097份,颁发证书630张。对于D类IVD,EURL需要参与性能验证和批检验。

在EURL监督范围内的168件D类申请中,虽然164件已签署主服务协议,但只有22件签订了具体的工作说明书,真正完成或安排性能验证的仅5件。
在批检验维度,有对应EURL的619件D类获证IVD中,实际由EURL完成批检验的只有279件。另有294件是通过替代实验室 (如独立测试机构) 完成的,这也是本次调查首次量化这一现象。
简言之:EURL的通量严重不足。制造商即使通过了NB审核,也可能因等不到EURL的测试排期而无法获证或销售。
进一步看,EURL目前仅覆盖肝炎/逆转录病毒感染、呼吸道病毒感染、疱疹病毒感染、血液标记物、细菌病原体感染、寄生虫感染六类 (官网数据2025年12月更新)。大量D类IVD甚至还没有对应的EURL,此等IVD的认证路径更具挑战。
丨认证周期隐性拉长是常态
报告中IVDR部分未直接给出从申请到发证的平均月数,但可以从多个间接指标拼凑出合理的估算。
如下图所示:在大多数情况下,从IVDR申请提交到与NB签署书面协议的时间少于2个月。整体而言,时间可接受。
从提交申请到签署书面协议的平均时间
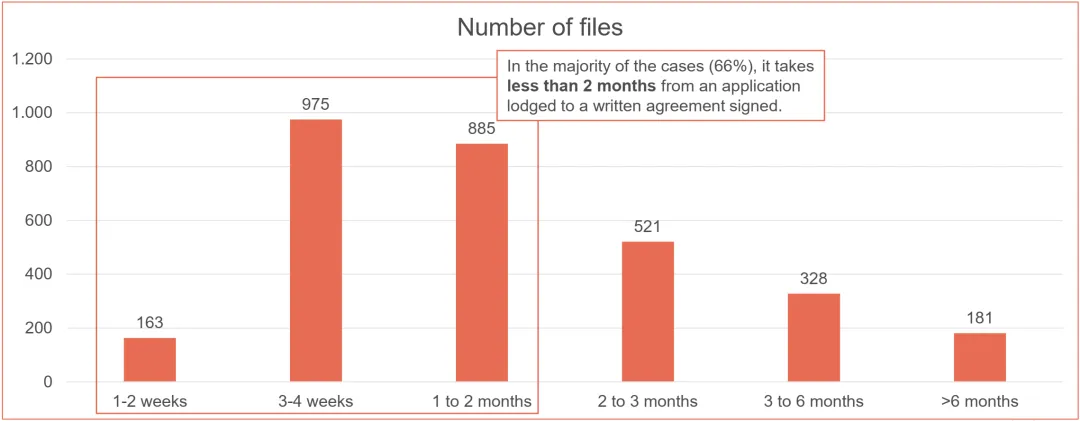
然而,从签约到获证则是另一番场景。如下图:截至2025年10月,IVDR申请总数3634件,证书合计2194件。基于12家NB的数据,对于QMS+产品证书,从签署书面协议到颁发新IVDR证书的时间,75%的NB需要13-18个月,8%的NB需要19-24个月。
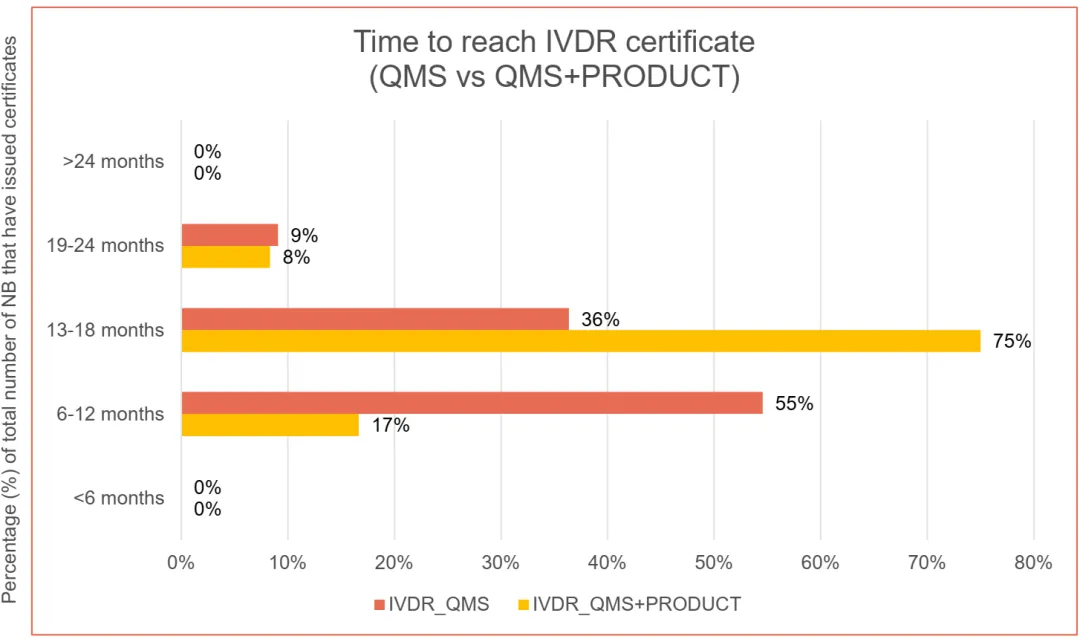
不考虑自企业立项始的内部准备周期,仅NB介入后的外部流程就可以年计算。对于习惯了IVDD自我声明这类数周便能走完流程的企业而言,快速易得的海外“严”监管认证已一去不返。

丨从被动应对到主动布局
IVDR生效至今已近四载,仍有不少企业沉醉于IVDD的价值余温 (仅需简单备案,许多LMIC快速准入) IVD企业出海 - IVDD指令的后遗症。然而,随着全球主流准入体系纷纷收紧 (例如,国内GMP新规发布、FDA QSPR实施、IVD WHO PQ改版、IVDR C类过渡期迫近),IVD制造商唯有从被动应对转向主动布局才有可能在激烈的行业整合中搏出生路。对此,方糖有五点建议如下:
立即提升技术文档质量
对照IVDR 附录II和III的要求,逐项检查技术文档:设备描述、性能评估 (分析性能和临床性能)、稳定性研究、风险管理、PMS计划……每个部分都必须有清晰的数据和逻辑支撑。
强烈建议引入熟悉IVDR的法规顾问或第三方机构进行预审。预审的花费,远比拒签后重来的成本低得多。
D类IVD定制化EURL策略
尽早确认旗下产品是否属于现有或即将扩展的EURL监督范围。不要被动等待NB通知,应主动联系对应的EURL,签署主服务协议,并尽早排期性能验证。
若EURL排期过长,主动向NB询问是否可以使用指定的替代实验室,并保留所有书面沟通记录。同时,考虑循序渐进的阶段认证策略:先申请低/中风险的B/C类设备 ,积累获证经验,再推进D类。
精明选择NB,优化认证路径
不同NB在D类及与EURL合作上的经验差异很大。优先选择已成功发放过D类证书、并与EURL有顺畅合作的机构。同时,要关注NB自身的资质稳定性。NB资质并非永久有效。遴选时,不仅要看NB的当前指定范围,还要评估其长期稳定性和应对新规的能力,规避可能在未来退出市场的机构。
与NB一道明确最合适的认证路径。对于大多数D类产品,附录IX (QMS+产品评估) 是主流选择。但针对高度外包或高度定制等类型的产品,也可考虑附录X+XI路径,但须确认EURL有足够的批次测试能力。
做好时间和财务的长期准备
制定一个18–30个月的认证路线图,并为EURL环节单独预留6–12个月的缓冲。财务上,除NB审核费,还要预算EURL测试费、替代实验室费用、法规顾问费及可能的翻译和整改费用。
选择合适的欧代 (价格,专业度,与NB关系,实验室资源等),确保其真正熟悉IVDR并能助力企业与NB、EURL沟通。
密切关注法规动态并保留备选方案
欧盟计划扩展EURL的覆盖范围,未来或有新的病原体类别或IVD类型被纳入强制监督。及时关注MDCG指南和EURL能力建设进展,必要时调整产品分类 (例如新冠产品降级) 及注册策略。
若IVDR的周期过于冗长,可同步规划英国UKCA认证或其他市场 (如东南亚、中东) 准入,以分散风险。

IVDR不是旧法规的简单升级,而是一场彻底的合规革命。对于制造商来说,既是挑战,也是行业洗牌的机会。
先行者,过往几年或已筑起竞争壁垒;迟疑守旧者,只会逐张丢失欧盟入场券。IVDR不是终点,而是全球监管趋同的缩影,是挑战WHO PQ等更高难度准入的演练场。主动布局,赢得的不只是证书,而是下一个十年的入场资格。